第四部:無機化学の基礎 金属元素(遷移元素)
☆ “ホーム” ⇒ “生活の中の科学“ ⇒ “基礎化学(目次)“ ⇒
ここでは,遷移元素周期表 4族の金属元素について, 【周期表 4族とは】, 【チタン】, 【ジルコニウム】, 【ハフニウム】, 【ラザホージウム】 に項目を分けて紹介する。
周期表 4族とは
周期表 4族に分類される元素のチタン( Ti ),ジルコニウム( Zr ),ハフニウム( Hf ),ラサホージウム( Rf )の概要を紹介する。
なお,実用材料などに利用される主な元素を太字で示した。また,これらの元素は,レアメタルに分類される。
次表には,これらの中から実用に供され元素の基礎物性を紹介する。比較のため,身近な金属単体として,アルミニウム,鉄の値も併記する。
なお,ポーリングの電気陰性度,イオン化エネルギーは別途紹介している。なお,これらの値は,算出に用いる解離エネルギー値や結合エネルギー値の改訂で変わるので,紹介した値は最新値ではなく,引用文献での値である。
【参考】
レアメタル( rare metal )
希少金属ともいわれ,以下の ①~④ のどれか一項目を満たし,かつ ⑤ の条件にあてはまるものをいう。
① 存在する量が少ない
② 鉱床を作らず,広く薄く分布している
③ 鉱床を作っても,特定の国や地域に限定されている
④ 鉱物からの取り出し,精製が難しい
⑤ 現代の産業に欠かせない素材である
レアメタル以外の金属はコモンメタル( common metal :汎用金属)という。チタン( Ti )のように,④と⑤でレアメタルに分類される元素は,精錬技術の向上などによりレアメタルからコモンメタルに変更される可能性がある。
| 元素記号 | Ti | Zr | Hf | Al | Fe |
|---|---|---|---|---|---|
| 原子番号 | 22 | 40 | 72 | 13 | 26 |
| 原子量 | 47.867 | 91.224 | 178.49 | 26.98 | 55.85 |
| 融点(℃) | 1668 | 1855 | 2233 | 660.3 | 1538 |
| 密度(×106 gm-3) | 4.506 | 6.52 | 13.31 | 2.70 | 7.87 |
| 結晶構造 | hcp | hcp | hcp | fcc | bcc |
| 格子定数(×10-10 m) | 2.950 , 4.686 | 3.232 , 5.147 | 3.197 , 5.058 | 4.0496 | 2.867 |
| モース硬度 | 6.0 | 5.0 | 5.5 | 2.8 | 4.0 |
| 電気抵抗(×10-8 Ωm:20℃) | 42 | 42.1 | 33.1 | 2.82 | 9.61 |
| 熱伝導率( W m-1K-1:300K) | 21.9 | 22.6 | 23 | 237 | 80.4 |
備考: hcp (六方最密充填,ちよう密六方),fcc (立方最密充填,面心立方格子),bcc (体心立方格子)
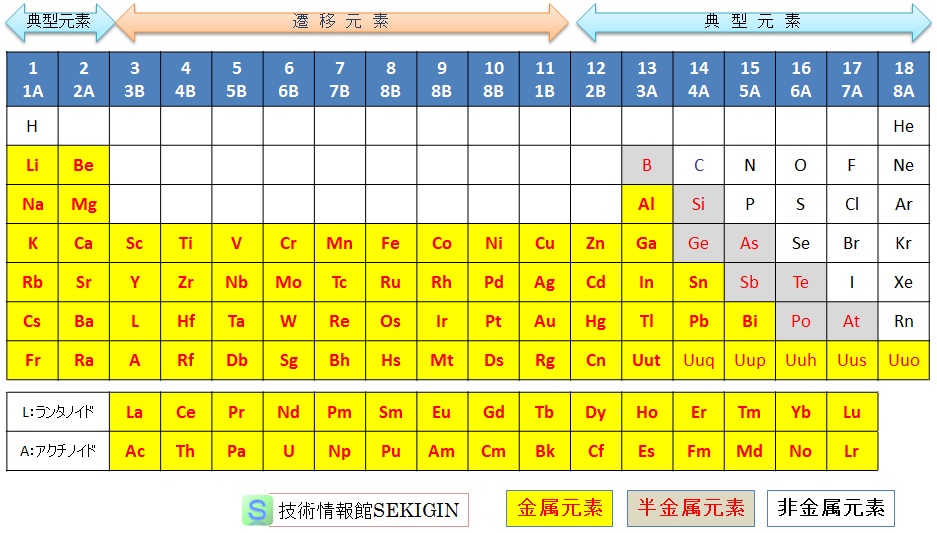
周期表(2015年)
ページの先頭へ
チタン( Ti )
チタンは,遷移元素の中で鉄に次ぐ2番目に多い元素で,化合物として地球上に広く分布している。チタン鉄鉱(イルメナイト: FeTiO3 ),金紅(きんこう)石(ルチル: TiO2 ),鋭錐(えいすい)石(アナタース: TiO2 ),板チタン石( TiO2 ),灰チタン石(ペロブスカイト: CaTiO3 ),くさび石(チタナイト: CaTiSiO5 )などがチタンを含む主な鉱物である。
チタンの生産では,主にチタン鉄鉱と金紅石が用いられる。これらの鉱石から炭素,塩素を用いて,塩化チタン(Ⅳ) TiCl4 を製造する。塩化チタンは,沸点136℃と低いので,容易に蒸留精製される。
塩化チタンをアルゴン気流中でマグネシウムと共に約900℃に加熱し,塩化マグネシウムとして塩素を除く(還元)ことで多孔質の金属チタン(スポンジチタン)が得られる。この方法をクロール法という,
TiCl4 + 2Mg → Ti + 2MgCl2
単体の物性
常温・常圧で六方最密充填構造( hcp )が安定で,880℃以上で体心立方構造( bcc )に転移する。延性・展性があり(加工性がある),機械強度も比較的大きい(硬くかつ粘り強い)金属である。
例えば,ヤング率は,チタン 115.7GPa(ギガパスカル),アルミニウム 70.3 GPa ,銅 129.8 GPa ,軟鉄 211.4 GPa ,鋳鉄 152.3 GPa である。
引張り強さは,材料加工技術などの影響を受けるので,JIS 規格値等などに見られる最小値を示すと,純チタン 270MPa 以上,純アルミニウム 60MPa 以上,純鉄 約 200MPa 以上, 無酸素銅 195MPa 以上と,構造材に用いられる一般的な材料と比較しても遜色ない機械的特性を有する。
チタン単体は,鉄と同等以上の強度を持つ一方,密度が鉄の約 57%と軽い。一方,軽い金属の代表であるアルミニウムは,チタンの密度の約 60%と軽いが,強度が半分以下である。すなわち,同じ引張り強さで比較すると,チタン製部品はアルミニウム製部品より軽くできる可能性がある。
【参考】
ヤング率( Young's modulus )
固体中の引張り又は圧縮応力とその方向における歪み(ひずみ:単位長さ当たりの伸び又は縮み)の比。物質特有の定数,単位はパスカル( P )又はニュートン毎平方メートル(広辞苑)。
すなわち,フックの法則( Hooke's law )が成立する弾性範囲で,ひずみと応力の比例定数をいう。フックの法則は,ばねの伸びと弾性限度以下の荷重は正比例するという近似的な法則である。弾性の法則とも呼ばれ,次式で表される。
ひずみ(ε)= 応力(σ)/ヤング率(E)
反応性
チタン単体は,中性水や常温の空気中では,表面が非常に薄く( nm オーダー)強固な酸化物(あるいは水酸化物)の被膜(不動態被膜)で覆われ,その後の酸化還元反応が抑制される。
チタンの不動態被膜は,加熱した濃硫酸,リン酸,塩酸には溶解するが,常温では通常の酸や塩基とはほとんど反応しない。
常温・常圧では,白金や金とほぼ同等の耐食性を持ち,酸や海水などに対しても高い耐食性を示す。しかし,高温では多くの元素と反応しやすいので,鋳造・溶接などの工程では酸素・窒素の遮断が必要になる。
用途例
金属素材としての用途
金属チタン及びその合金は,製錬・加工が難しく,高価であるが,強度・軽さ・耐食性・耐熱性に優れているため,航空機,潜水艦,自転車,化学プラント,生体インプラント材料など多くの分野で使用されている。
特に戦闘機では,コストより性能を重視するので,軽量化を目的に多量に使われていた。例えば,ステルス戦闘機の F-22 では,機体重量の 50%以上がチタン合金である。
チタンやチタン合金に関する製品規格 JIS H 4600 「チタン及びチタン合金−板及び条 :Titanium and titanium alloys-Sheets, plates and strips 」では,化学成分,機械的性質,形状等により種類と品質を規定している。なお,条とは断面が長方形の圧延材をいう。
この規格では,純チタン 4 種類(形成加工用 1 種,汎用 2 種,中強度 3 種,高強度 4 種),チタン合金に関しては,耐食チタン合金 13 種類( 11 種~ 23 種),α合金( 50 種),α-β合金 4 種類( 60 種,60E 種,61 種,61F 種),β合金( 80 種)に分類している。
化合物としての用途例
酸化チタン(Ⅳ)
チタンの約 95%は酸化チタン(Ⅳ)TiO2 として用いられている。
日本での酸化チタン(Ⅳ)の工業的製法は,チタン鉄鉱(イルメナイト鉱石: FeTiO3 )を原料に,濃硫酸の処理でオキシ硫酸チタン( TiOSO4 )とし,これを加水分解して得られたオキシ水酸化チタン( TiO(OH)2 )を焼成することで酸化チタンを得る。
酸化チタン(Ⅳ)の結晶構造には,アナターゼ型(正方晶),ルチル型(正方晶),ブルッカイト型(斜方晶)の三種類がある。アナターゼ型を 900℃以上に,ブルッカイト型を 650℃以上に加熱すると安定構造であるルチル型に転移する。
酸化チタン(Ⅳ)は,ふっ化水素酸,熱濃硫酸および溶融アルカリ塩に溶解するが,それ以外の酸,塩基,水および有機溶剤には溶解しない。
アナターゼ型酸化チタン(Ⅳ)
387nm 短い波長の光(紫外線)を吸収すると,価電子帯の電子が伝導帯に励起され自由電子と正孔を生成する。正孔の酸化力は非常に強く,例えば水と反応すると活性酸素種が生成される。これを,酸化チタンの光触媒作用という。
活性酸素種は一般に非常に強い酸化力をもち,化学薬品や細菌などに対して分解作用を示す。病院などの壁や床を酸化チタンでコーティングすることで,紫外線ランプの照射で殺菌処理することができる。
光を照射すると導電化する性質を利用し,オフセット印刷の感光体として用いられている。酸化亜鉛を利用した従来のものよりも耐久性が高く,解像度も高い特徴がある。
ルチル型酸化チタン(Ⅳ)
光触媒作用はないが,400nmよりも短波長の光を強く吸収する一方で,可視光の透過性が大きいため,日焼け止めを目的とした化粧品に使われる。また,屈折率がダイヤモンドより大きく,熱安定性,耐久性が高いので,鮮やかな白顔料(チタン白,チタニウムホワイトと称す)として,塗料,絵具や合成樹脂などに使用される。
さらには,人体への影響が小さいと考えられ,食品,医薬品,化粧品の着色料(食品添加物)として,紙に織り込むことで,白く丈夫で透けない良質の紙として利用されている。
その他の化合物
チタン酸バリウム:強誘電性を示すセラミックス,コンデンサ材料,焦電体,圧電体などの代表的な電子部品材料
チタン酸ストロンチウム:半導体として,バリスタ,センサー,熱電素子など,ダイヤモンド類似石として人工宝石や光学材料
塩化チタン(Ⅳ):煙幕(高湿度の空気中で発煙する)
ページの先頭へ
ジルコニウム( Zr )
天然には,ジルコン( ZrSiO4 = ZrO2SiO2)として産出される。ジルコンは,風信子(ひあしんす)鉱ともいわれる。
ジルコニウムは,常温・常圧では六方最密充填構造( hcp:α型)が安定で,862℃以上で体心立方構造( bcc:β型)へ転移する金属である。
反応性
ジルコニウム単体は,常温・常圧の空気中では,表面が酸化物被膜で覆われ,その後の酸化が抑制される。
常温の酸・塩基に対して安定であるが,高温では,各種元素(酸素,窒素,水素,ハロゲンなど)と反応する。
用途例
ジルコニウムの熱中性子の吸収断面積が小さいので,原子炉の燃料を被覆する材料(燃料被覆管)として,ジルコニウム合金が用いられる。
酸化ジルコニウム(Ⅳ)( ZrO2 )は,ジルコニアとも呼ばれ,白色顔料,皮膚炎の治療薬,圧電素子,コンデンサ,ガラス,宝飾品(模造ダイヤ),差し歯のブリッジなどに用いられる。
ページの先頭へ
ハフニウム( Hf )
天然には,ジルコンのZrの一部をハフニウム Hf に置換されたハフノン( HfSiO4 )が固溶した鉱物として産出される。日本では,ジルコンの変種で,ハフニウムを比較的多く含む苗木(なえぎ)石が産出される。
ハフニウムは,常温・常圧で六方最密充填構造( hcp )が安定な金属である。
反応性
ハフニウム単体は,展性・延性に富み,常温・常圧では酸化力のある酸に溶解するが,塩基には溶解しない。
高温では,各種元素(酸素,窒素,水素,ハロゲンなど)と反応する。
用途例
ハフニウムは,ジルコンとは逆に熱中性子の吸収断面積が大きく,原子炉の制御棒用材料として用いられる。
酸化ハフニウム(Ⅳ)HfO2 は,高誘電率材料,酸化環境下でのプラズマ電極などの絶縁性耐熱材に用いられる。
ページの先頭へ
ラザホージウム( Rf )
ラザホージウムは,原子番号 104 ,原子量 (261) の安定同位体を持たず,天然には存在しない元素である。
カリフォルニア大学バークレー校で人工的に作ったと考えられている。元素名は長らく決められず,ウンニルクアジウム (Unq) と呼ばれていたが,物理学者アーネスト・ラザフォードのに由来するラザホージウムをIUPACが正式名称として承認した。
ラザホージウムの化学的性質は,ジルコニウムやハフニウムに類似していることが知られている。
ページの先頭へ