第四部:無機化学の基礎 金属元素(典型元素)
☆ “ホーム” ⇒ “生活の中の科学“ ⇒ “基礎化学(目次)“ ⇒
ここでは,周期表 12族の金属元素について, 【周期表 12族とは】, 【亜鉛】, 【カドミウム】, 【水銀・コペルシウム】 に項目を分けて紹介する。
周期表 12族とは
周期表 12 族の亜鉛( Zn ),カドミウム( Cd ),水銀( Hg ),コペルニシウム( Cn )は,典型元素の金属元素に分類される。
なお,太字は実用される元素で,亜鉛は必須ミネラルに分類される元素である。原子番号 112 のコペルニシウムは,人工放射性物質で実用例のない元素である。
次には,実用される周期表 12 族元素(単体)の基礎物性を紹介する。なお,比較のため,身近な金属単体として,アルミニウム,鉄,銅の値も併記する。
なお,ポーリングの電気陰性度,イオン化エネルギーは別途紹介している。なお,これらの値は,算出に用いる解離エネルギー値や結合エネルギー値の改訂で変わるので,紹介した値は最新値ではなく,引用文献での値である。
| 元素記号 | Zn | Cd | Hg | Al | Fe | Cu |
|---|---|---|---|---|---|---|
| 原子番号 | 30 | 48 | 80 | 13 | 26 | 29 |
| 原子量 | 65.38 | 112.11 | 200.59 | 26.98 | 55.85 | 63.55 |
| 融点(℃) | 419.53 | 321.07 | -38.83 | 660.3 | 1538 | 1084 |
| 密度(×106 gm-3) | 7.14 | 8.65 | 13.53* | 2.70 | 7.87 | 8.94 |
| 結晶構造 | hcp | hcp | - | fcc | bcc | fcc |
| 格子定数(×10-10 m) | 2.659 , 4.937 | 2.979 , 5.618 | - | 4.0496 | 2.867 | 3.615 |
| モース硬度 | 2.5 | 2.0 | - | 2.8 | 4.0 | 3.0 |
| 電気抵抗(×10-8 Ωm:20℃) | 5.90 | 7.27 | 96.1* | 2.82 | 9.61 | 1.68 |
| 熱伝導率( W m-1K-1:300K) | 116 | 96.6 | 8.3 | 237 | 80.4 | 401 |
備考: hcp (六方最密充填,ちよう密六方),fcc (立方最密充填,面心立方格子),bcc (体心立方格子)
*:水銀の密度は融点付近の液体密度,電気抵抗率は25℃,
【参考】
四大公害病
水俣病:熊本県チッソ水俣工場,1956年熊本県水俣湾,有機水銀による水質汚染や底質汚染
第二水俣病(新潟水俣病):新潟県昭和電工鹿瀬工場,1964年新潟県阿賀野川流域,有機水銀による水質汚染や底質汚染
四日市ぜんそく:三重県四日市コンビナート,1960年から1972年三重県四日市市,亜硫酸ガスによる大気汚染
イタイイタイ病:岐阜県三井金属鉱業神岡事業所(神岡鉱山),1910年代から1970年代前半に富山県神通川流域,カドミウムによる水質汚染
必須ミネラル
健康増進法(平成 14年法律第 103 号)に基づき厚生労働大臣が定める「日本人の食事摂取基準(2015年版)」 に基準摂取量が定められているミネラルをいう。必要所要量の違いで,主要ミネラル 7 種,微量ミネラル 9 種に分けられる。
主要ミネラル( 100 mg /1日 以上):硫黄 S(骨・軟骨・皮膚・髪の毛・爪など),塩素 Cl(胃液中の胃酸),ナトリウム Na(血液・体液の浸透圧を調整),カリウム K( 血圧の上昇抑制,利尿作用),マグネシウム Mg(骨や歯の強か,酵素の補助),カルシウム Ca(骨・歯の成分,エネルギー代謝),リン P(骨・歯の成分,代謝の補助)
微量ミネラル( 100 mg /1日 未満): 鉄 Fe(赤血球のヘモグロビン),亜鉛 Zn(生殖機能,ホルモン合成),銅 Cu(ヘモグロビン生成,骨格成分),マンガン Mn(骨や関節),ヨウ素 I(甲状腺ホルモン,代謝),セレン Se(抗酸化力,老化防止),モリブデン Mo(肝臓,腎臓の老廃物分解),クロム Cr(糖の代謝),フッ素 F(虫歯予防)
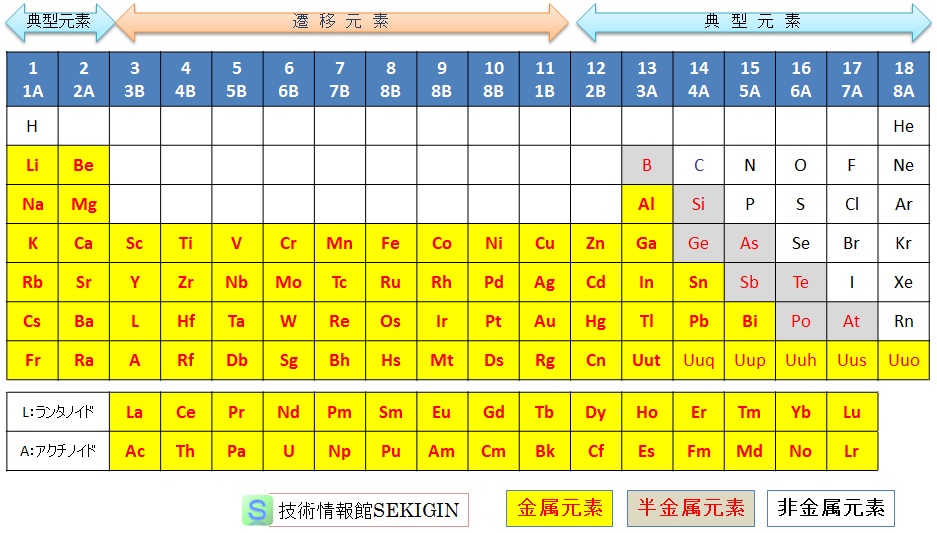
周期表(2015年)
ページの先頭へ
亜鉛( Zn )
日本人の食事摂取基準(2015年版)に定める必須ミネラル 16 種の一つで,天然に元素鉱物(金属鉱物)で稀に産出されることはあるが,主には硫化鉱物の閃亜鉛鉱(せんあえんこう: ZnS )や結晶構造の異なるウルツ鉱( ZnS ),炭酸塩鉱物の菱亜鉛鉱(りょうあえんこう: ZnCO3 )などから産出される。
単体の製造では,亜鉛の沸点が低く( 907℃)気化し易いので,還元して気化した亜鉛を分別蒸留する方法,硫酸亜鉛の水溶液として電気分解する方法が用いられる。
大気中での反応
単体は,中性の水や常温の空気中では,酸素,水,二酸化炭素と反応し,酸化亜鉛( ZnO )の他に塩基性炭酸亜鉛( 2ZnCO3・3Zn(OH)2 )などの難溶性塩が生成し,金属表面がこれらで覆われると,酸化反応が抑制される。
酸との反応
酸に対しては,例えば
Zn + H2SO4 ( 2H+ + SO42- ) → ZnSO4 ( Zn2+ + SO42- ) + H2↑
と,激しく水素を発生する酸化反応が起きる。
酸化性のある希硝酸の場合は,濃度により,水素以外に亜酸化窒素( NO ),窒素( N2 )やアンモニウムイオン( NH4+ )を生成する。
塩基との反応
強塩基に対しても,次に示すように,テトラヒドロキシド亜鉛(Ⅱ)酸イオン( Zn(OH)42- )を生成して溶解するので両性金属(元素)と呼ばれる。
Zn + 2NaOH ( Na+ + OH- ) + 2H2O → Na2Zn(OH)4 ( Na+ + Zn(OH)42- ) + H2↑
亜鉛化合物の反応性
亜鉛の酸化物( ZnO )や水酸化物( Zn(OH)2 )は,酸や強塩基と反応して,単体の亜鉛の反応生成物と同じテトラヒドロキシド亜鉛(Ⅱ)酸塩を作るので,アルミニウム,スズや鉛と同様に,両性酸化物,両性水酸化物と呼ばれる。
例えば,亜鉛イオンを含む水溶液に,少量の塩基を添加すると,不溶性(難溶性)の水酸化亜鉛( Zn(OH)2 )として沈殿するが,
Zn2+ + 2OH- → Zn(OH)2↓
これに,過剰の塩基が加わると,水酸化亜鉛は,テトラヒドロキシド亜鉛(Ⅱ)酸イオン( Zn(OH)42- )として溶解する。
Zn(OH)2 + 2OH- → Zn(OH)42-
亜鉛イオンを含む中性又は塩基性の水溶液に,硫化水素を通じた時,不溶性(難溶性)の硫化亜鉛( ZnS )として白色沈澱が生じる。この反応は,水質検査における亜鉛イオンの検出に利用されている。
Zn2+ + H2S + 2OH- → ZnS↓ + H2O
用途例
金属素材としての用途
亜鉛の単体は,マンガン電池,アルカリ電池などの負極材料として使用されている。鉄(鋼)との標準酸化還元電位の差を利用した電気防食における流電陽極として,船舶や水道鋼管の防食目的に亜鉛ブロックのままで用いられる。
同じ原理を利用して鋼の腐食抑制を目的としためっき(溶融亜鉛めっき,電気亜鉛めっき)鋼板が建築分野,土木分野で広く用いられている。
亜鉛合金は融点が低く,優れた機械的特性(寸法精度,耐衝撃性など)のため,黄銅(真鍮ともいう:銅と亜鉛の合金),洋銀(銅,亜鉛,ニッケルの合金),カラーゴールド(金,銀,亜鉛の合金)やダイカスト製品(ダイキャストともいう:亜鉛,アルミニウム,マグネシウムなどとの合金)として利用されている。
蛇足:トタンは薄板の電気亜鉛めっき鋼板を,ブリキは薄板の電気錫(スズ)めっき鋼板をいう。
化合物として用途
酸化亜鉛(亜鉛華ともいう)は,白色の顔料,医薬品,化粧品などに用いられる。
亜鉛化合物は,必須ミネラル摂取を目的とした健康食品やサプリメントにも用いられている。
ページの先頭へ
カドミウム( Cd )
亜鉛鉱に含まれ,亜鉛精錬の際に副産物として,亜鉛精錬の際に同時に得られる。
カドミウムは,有害物質(腎臓機能に障害,発がん性)として認識され,過去にはカドミウムによる環境汚染(四大公害病の一つイタイイタイ病)が問題となった。
反応性
単体は,軟らかく展性に富む金属,湿度の高い空気中で徐々に酸化され金属光沢を失う。塩酸,希硫酸とは徐々に反応する。希薄な塩基性水溶液とはほとんど反応しない。
用途例
融点 70 ℃程度の低融点合金(ウッド合金)の成分( Bi 50 % , Pb 26.7 % , Sn 13.3 % , Cd 10 % )として用いられる。
水酸化カドミウム( Cd (OH)2 )は,ニッケル・カドミウム蓄電池(ニッカド電池)の負極活性剤として用いられる。
硫化カドミウム( CdS )は黄色顔料(カドミウムイエロー)や半導体などに,セレン化カドミウム( CdSe )は,赤色顔料(カドミウムレッド)や半導体などに用いられるが,近年は,毒性を嫌い,代替品のある場合は使用を忌避する傾向が強い。
ページの先頭へ
水銀・コペルニシウム
水銀( Hg )
常温,常圧で液状の金属元素で,硫化物の辰砂(しんしゃ,HgS ,別名賢者の石),単体の自然水銀として産出する。
常温の空気中及び水との接触では,酸化還元反応が起きず,安定に存在できる。水銀は他の金属との合金を作り易く,常温で液体になるものが多い。この合金をアマルガム( amalgam )という。
反応性
酸化性のない酸には溶解しないが,酸化性の酸(硝酸や熱濃硫酸など)で溶解する。
希硝酸に対しては,
3Hg + 8HNO3 ( H+ + NO3- ) → 3Hg(NO3)2 ( Hg2+ + 2NO3- ) + 2NO↑+ 4H2O
と一酸化窒素を発生し,
濃硝酸に対しては,
Hg + 4HNO3 ( H+ + NO3- ) → Hg(NO3)2 ( Hg2+ + 2NO3- ) + 2NO2↑+ 2H2O
と二酸化窒素を発生し,
熱濃硫酸に対しては,
Hg + 2H2SO4 ( 2H+ + SO42- ) → HgSO4 ( Hg2+ + SO42- ) + SO2↑+ 2H2O
と二酸化硫黄を発生し溶解する。
用途例
単体は,比重が大きく,電気伝導性のある液体として,温度計(水銀温度計),圧力計(気圧計,血圧計),水銀スイッチに,水銀蒸気として蛍光灯,水銀ランプなどに用いられていた。
アマルガムは,歯科治療用に銀とスズの合金に銅や亜鉛を添加した粉末を水銀で練った銀スズアマルガムが用いられていた。古くは,金の精製や金めっきに水銀を用い金のアマルガムにした後,加熱し水銀を蒸発する方法が用いられていた。
水銀化合物は,古来より,硫化水銀( HgS )の赤を利用した朱肉や釉薬として,塩化第二水銀( HgCl2 )の毒性を利用した消毒薬,メチル水銀などの有機水銀は,毒性を利用した農薬や化学工業での触媒として用いられていたが,有機水銀汚染による水俣病を契機に使用が制限,自粛されている。
コペルニシウム( Cn )
ドイツの重イオン研究所で加速器を用いて,亜鉛イオンと鉛イオンの衝突で合成した元素である。元素名は,科学者コペルニクスにちなんで命名された。
ページの先頭へ