第四部:無機化学の基礎 金属元素(遷移元素)
☆ “ホーム” ⇒ “生活の中の科学“ ⇒ “基礎化学(目次)“ ⇒
ここでは,遷移元素周期表 11族の金属元素について, 【周期表 11族について】, 【銅】, 【銀】, 【金】, 【ダームスタチウム】 に項目を分けて紹介する。
周期表 11族について
周期表 11族に分類される元素,銅( Cu ),銀( Ag ),金( Au ),レントゲニウム( Rg )の概要を紹介する。
なお,実用材料などに利用される主な元素を太字で示した。また,銅は,必須ミネラルに分類される元素である。
次表には,これらの中から実用に供され元素の基礎物性を紹介する。比較のため,身近な金属単体として,アルミニウム,鉄の値も併記する。
なお,ポーリングの電気陰性度,イオン化エネルギーは別途紹介している。なお,これらの値は,算出に用いる解離エネルギー値や結合エネルギー値の改訂で変わるので,紹介した値は最新値ではなく,引用文献での値である。
【参考】
必須ミネラル
健康増進法(平成 14年法律第 103 号)に基づき厚生労働大臣が定める「日本人の食事摂取基準(2015年版)」 に基準摂取量が定められているミネラルをいう。必要所要量の違いで,主要ミネラル 7 種,微量ミネラル 9 種に分けられる。
主要ミネラル( 100 mg /1日 以上):硫黄 S(骨・軟骨・皮膚・髪の毛・爪など),塩素 Cl(胃液中の胃酸),ナトリウム Na(血液・体液の浸透圧を調整),カリウム K( 血圧の上昇抑制,利尿作用),マグネシウム Mg(骨や歯の強か,酵素の補助),カルシウム Ca(骨・歯の成分,エネルギー代謝),リン P(骨・歯の成分,代謝の補助)
微量ミネラル( 100 mg /1日 未満): 鉄 Fe(赤血球のヘモグロビン),亜鉛 Zn(生殖機能,ホルモン合成),銅 Cu(ヘモグロビン生成,骨格成分),マンガン Mn(骨や関節),ヨウ素 I(甲状腺ホルモン,代謝),セレン Se(抗酸化力,老化防止),モリブデン Mo(肝臓,腎臓の老廃物分解),クロム Cr(糖の代謝),フッ素 F(虫歯予防)
| 元素記号 | Cu | Ag | Au | Al | Fe |
|---|---|---|---|---|---|
| 原子番号 | 29 | 47 | 79 | 13 | 26 |
| 原子量 | 63.55 | 107.87 | 196.97 | 26.98 | 55.85 |
| 融点(℃) | 1084.6 | 961.8 | 1064.2 | 660.3 | 1538 |
| 密度(×106 gm-3) | 8.94 | 10.49 | 19.30 | 2.70 | 7.87 |
| 結晶構造 | fcc | fcc | fcc | fcc | bcc |
| 格子定数(×10-10 m) | 3.615 | 4.086 | 4.078 | 4.0496 | 2.867 |
| モース硬度 | 3.0 | 2.5 | 2.5 | 2.8 | 4.0 |
| 電気抵抗(×10-8 Ωm:20℃) | 1.678 | 1.587 | 2.214 | 2.82 | 9.61 |
| 熱伝導率( W m-1K-1:300K) | 401 | 429 | 318 | 237 | 80.4 |
備考: fcc (立方最密充填,面心立方格子),bcc (体心立方格子)
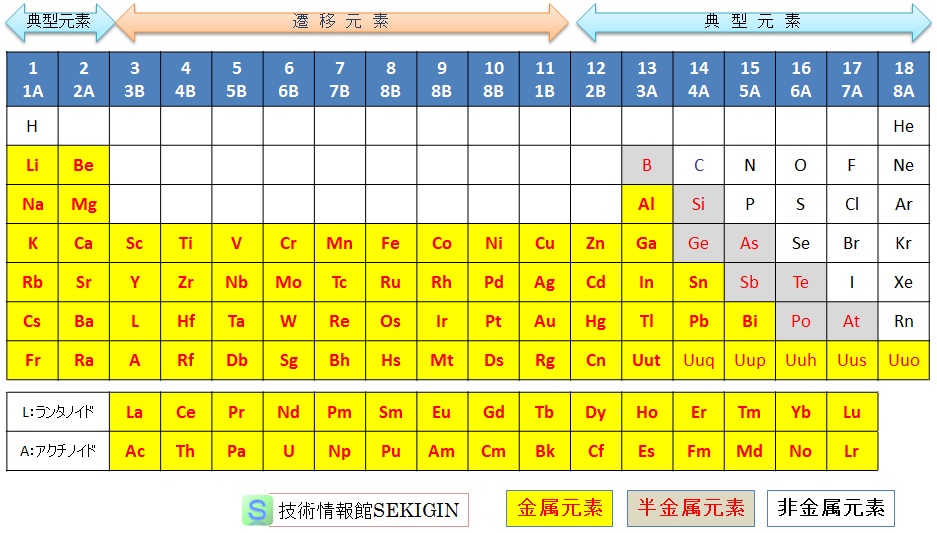
周期表(2015年)
ページの先頭へ
銅( Cu )
銅は,クラーク数 0.01 で 25 位と,クロム( 21 位),ニッケル( 24 位)より存在量は少ないが,比較的容易に精製できたため,古代より利用されてきた金属である。。
銅の製造では,古くは自然銅( Cu )が利用され,需要の伸びと共に,赤銅鉱(せきどうこう: Cu2O ),黒銅鉱(こくどうこう: CuO ),孔雀石(くじゃくいし,マラカイト: Cu2(CO3)(OH)2 )などの酸化銅を含む鉱物が利用された。
銅の生産
銅鉱床
現在は,斑岩銅鉱床(はんがんどうこうしょう)から全生産量の半数以上が得られている。斑岩銅鉱床とは,花こう岩質のマグマが地殻の浅い所まで貫入し,熱水変質を受けて形成した熱水性鉱床をいい,銅や金,モリブデンが低品位ではあるが広範囲に含まれ,鉱床の規模が極めて大きいことが特徴である。
鉱床には,黄銅鉱(おうどうこう,キャルコパイライト:CuFeS2 )と黄鉄鉱( FeS2 )を主とし,輝水鉛鉱(きすいえんこう: MoS2 ),自然金( Au ),輝銅鉱(きどうこう,カルコサイト: Cu2S ),孔雀石,珪孔雀石(けいくじゃくせき,クリソコラ: Cu2H2Si2O5(OH)4 ),アタカマ鉱( Cu2(OH)3Cl )などが伴われる。
天然の銅の鉱石は,16 種類以上にも及ぶ。上記以外の主な鉱物は次の通りである。
酸化鉱物 :藍銅鉱(らんどうこう,アズライト),胆礬(たんぱん,カルカンサイト),ブロシャン銅鉱
硫化鉱物 :斑銅鉱(はんどうこう),硫砒銅鉱(りゅうひどうこう),銅藍(どうらん,コベリン),安四面銅鉱(あんしめんどうこう,テトラヘッドライト),方輝銅鉱(ほうきどうこう),ヌクンダム鉱,キューバ鉱,砒四面銅鉱(ひしめんどうこう,テナンタイト),ルソン銅鉱,ファマチナ鉱,三原鉱(みはらこう)
銅の製錬
銅鉱石中の銅濃度は比較的低く,鉱石の大部分は硫化物である。鉱石粉砕後,泡沫浮選などで銅濃度を高め,これに,コークス,石灰石( CaCO3 ),ケイ砂( SiO2 )を加えて溶錬炉で溶融させる。これにより,鉱石中の不純物としての鉄はスラグとして除去され,硫化銅を主とする製品,銅鈹(どうかわ,銅マット)が得られる。
銅鈹を空気酸化しながら焙焼し,得られた酸化第一銅を高温( 2000℃以上)で還元し,粗銅(銅含有率約 98%)が得られる。粗銅の電解精錬によって得られた物を電気銅という。
電気銅をシャフト炉で溶解製錬する方法でタフピッチ銅が,リンなどの脱酸剤を加えて残留酸素を除去する方法で脱酸銅が,高真空中で溶解させることで酸素を除去する方法で無酸素銅が得られる。
銅単体の特性
銅単体は,面心立方構造が安定で,柔らかく展性,延性に優れ,電気抵抗率が低く,熱伝導率が高い,特有の色を持つ金属である。電気抵抗率及び熱伝導率は,金属単体の中では,銀に次ぎ 2番目の特性を有する。
灰色や銀白色以外の色を持つ金属元素は,銅(あかがね色),金(金色),オスミウム(青み)の3元素のみである。
反応性
銅単体の反応性
中性の水や常温の空気中では,銅単体の表面が,酸素,水,二酸化炭素,環境汚染因子などと反応し,生成した黒色の酸化銅(Ⅱ)( CuO ),青緑色の緑青( 塩基性炭酸銅 CuCO3・Cu(OH)2 ,塩基性塩化銅 CuCl2・Cu(OH)2 ,塩基性硫酸銅 CuSO4・Cu(OH)2 など)の比較的厚い層で覆われ,その後の酸化還元反応が抑制される。
酸化性のない酸には溶解しないが,酸化性の酸(硝酸や熱濃硫酸など)で溶解する。
希硝酸に対しては,一酸化窒素( NO )を発生して溶ける。
3Cu + 8HNO3 ( H+ + NO3- ) → 3Cu(NO3)2 ( Cu2+ + 2NO3- ) + 2NO↑+ 4H2O
濃硝酸に対しては,二酸化窒素( NO2 )を発生して溶ける。
Cu + 4HNO3 ( H+ + NO3- ) → Cu(NO3)2 ( Cu2+ + 2NO3- ) + 2NO2↑+ 2H2O
熱濃硫酸に対しては,二酸化硫黄( SO2 )を発生して溶ける。
Cu + 2H2SO4 ( 2H+ + SO42- ) → CuSO4( Cu2+ + SO42- ) + SO2↑+ 2H2O
銅化合物の反応性
黒色の酸化銅(Ⅱ)( CuO )を 1000℃以上に加熱すると,分解し,酸素( O2 )と赤褐色の酸化銅(Ⅰ)( Cu2O )が生成する。
硫酸銅(Ⅱ)( CuSO4 )を水に溶解すると,銅(Ⅱ)イオンは,水溶液中でテトラアクア銅(Ⅱ)イオン( Cu(H2O)42+ )として存在し,青色を呈する。この水溶液を自然乾燥すると,水和物として青色の硫酸銅(Ⅱ)五水和物( CuSO4・5H2O )が得られる。これを加熱すると,水和水が外れて硫酸銅(Ⅱ)無水物( CuSO4 )の白色粉末が得られる。
銅イオン( Cu2+ )を含む水溶液は,水酸化物イオン( OH- )との反応では,不溶性(難溶性)の水酸化銅(Ⅱ)( Cu(OH)2 )が沈殿する。アンモニア水では,形成した水酸化銅(Ⅱ)が過剰のアンモニア( NH3 )と反応し,銀イオンや亜鉛イオンと同様に,錯イオンのテトラアンミン銅(Ⅱ)イオン( Cu (NH3)42+ )を形成し溶解する。
銅イオンを含む水溶液に硫化水素( H2S )を通じると,黒色の硫化銅(Ⅱ)( CuS )が沈殿する。
用途例
銅単体の主要な用途として,導線(電線,配線に 60%),建材(屋根材,配管に 20%),産業機械( 15%)に利用され,銅合金(青銅や黄銅)の利用は 5%程度である。
銅合金には,錫との合金(青銅,ブロンズ)は美術品・装飾品などに,亜鉛との合金(黄銅,真鍮)は,金色の合金で釘・ねじ・建築資材・装飾品などに,ニッケルとの合金(白銅,洋白)は 50円,100円などの硬貨,食器,バイメタルなどに用いられている。
その他には,生物付着防止(養殖業),抗菌(木の防腐剤など)を目的とした用途がある。
銅は動植物の必須ミネラルである。銅が欠乏すると,鉄吸収量の低下による貧血,骨の異常,成長障害,骨粗鬆症などの障害に至る。
ページの先頭へ
銀( Ag )
銀の生産
銀鉱床
天然の銀を含む鉱石・鉱物は数多くある。その中で,金鉱石と銀鉱物が伴に存在することが多く,金銀鉱として採掘される。
銀は,まれに自然銀( 83.1~100 Ag重量%)や金との合金(エレクトラム: 5.7~83.1 Ag重量%)として産出されたが,多くは輝銀鉱(針銀鉱ともいう)Ag2S ,濃紅銀鉱 Ag3SbS3 ,淡紅銀鉱 Ag3AsS3 ,脆銀鉱 Ag5SbS4 ,マチルダ鉱 AgBiS2,輝銀銅鉱 AgCuS ,雑銀鉱 (AgCu)16Sb2S11 などの硫化物や多様な硫塩鉱物として産出された。
上記以外にも,銀の鉱石・鉱物が数多くある。主なものを次に紹介する。
硫化鉱物:硫セレン銀鉱,ミアジル鉱,スミス鉱,古遠部鉱(ふるとおべこう),パボン鉱,ピアス鉱,ダイアホル鉱,フライエスレーベン鉱,アンドール鉱,ラムドール鉱,フィゼリ鉱,含銀四面安銅鉱
テルル化鉱物:ヘッス鉱( Ag2Te ),エンプレス鉱,ペッツ鉱,シルバニア鉱( AuAgTe4 )
セレン化鉱物:ナウマン鉱( Ag2Se )
ハロゲン化鉱物:角銀鉱( AgCl ),臭銀鉱,沃銀鉱(ようぎんこう)
銀の精錬
銀の生産では,過去には銀を多く含む鉱石,例えば,輝銀鉱をシアン化カリウム( KCl )水溶液で溶解し,イオン化傾向の大きい金属との酸化還元反応で銀イオンを還元して得るなどの方法が主流であった。しかし,現在は,製錬技術の向上と共に,銅,鉛,亜鉛などの電解製錬工程での副産物として回収するのが主流となっている。
前出の銅精錬で溶材溶剤として用いるケイ砂( SiO2 )の代わりに金銀鉱を用いると,銅精錬過程で金・銀が粗銅に溶け込む。
粗銅の電気精錬過程で,金と銀は銅から分離され,ほぼ完全に回収することができる。
銀単体の特性
銀は,面心立方構造が安定で,柔らかく展性,延性に優れる貴金属に分類される金属である。延性,展性については,金に次ぐ特性を有する。
単体の電気抵抗率及び熱伝導率は,金属単体の中では最も優れた特性を有する。なお,熱伝導率は,最も高い炭素単体(ダイヤモンド 1000 ~ 2300 W m-1 K-1 :300K)に次いで高い。
また,可視光線の反射率が金属中で最大( 98%程度)のため,美しい金属光沢を有する。一般的に金属光沢を銀色と称するのはこのためである。
反応性
銀単体の反応性
銀単体は,中性の水や常温の空気中では,酸素,水とは反応しないが,貴金属の中では比較的化学変化しやすく,硫化物や塩化物が存在すると,単体表面に難溶性の黒色の硫化銀( Ag2S ),白色の塩化銀( AgCl )の薄い被膜を作る。
塩酸や希硫酸など酸化性のない酸には溶解しないが,酸化性の酸(硝酸や熱濃硫酸など)に溶解する。
希硝酸に対しては,一酸化窒素( NO )を発生して溶ける。
3Ag + 4HNO3 ( H+ + NO3- ) → 3AgNO3 ( Ag+ + NO3- ) + NO↑+ 2H2O
濃硝酸に対しては,二酸化窒素( NO2 )を発生して溶ける。
Ag + 2HNO3 ( H+ + NO3- ) → AgNO3 ( Ag+ + NO3- ) + NO2↑+ H2O
熱濃硫酸に対しては,二酸化硫黄( SO2 )を発生して溶ける。
2Ag + 2H2SO4 ( 2H+ + SO42- ) → Ag2SO4 ( 2Ag+ + SO42- ) + SO2↑+ 2H2O
銀化合物の反応性
銀イオン( Ag+ )を含む水溶液は,ハロゲンイオンと反応し,不溶性(難溶性)のハロゲン化銀( AgCl :白色,AgBr :淡い黄色,AgI :黄色)を生成する。
水酸化物イオン( OH- )との反応では,水酸化銀ではなく不溶性の酸化銀( Ag2O )を生成する。
アンモニア( NH3 )との反応では,銅イオンや亜鉛イオンと同様に,過剰のアンモニアと反応し,錯イオンのジアンミン銀(Ⅰ)イオン( Ag (NH3)2+ )を形成し溶解する。
錯イオン形成の他の例として,チオ硫酸イオン( S2O32- )とからビス(チオスルファト)銀(Ⅰ)イオン( Ag (S2O3)23- )の形成,シアンイオン( CN- )とからジシアニド銀(Ⅰ)酸イオン( Ag (CN)2- )の形成などがある。
用途例
金属素材としての用途
銀単体は,貴金属のなかでは比較的産出量も多く安価なため,日常生活の中で,シルバーアクセサリーとして用いられる。この場合,黒ずみを防ぐためロジウムなどのめっき処理が多い。
銀単体の黒ずみの原因は,大気中の硫化水素などとの反応生成物である黒色難溶性の硫化銀(Ⅰ)( 2Ag + H2S → Ag2S + H2 )が銀表面を覆うためである。温泉に入るとき,銀アクセサリーを外すように言われるのはこのためである。
また,ナイフ,フォーク,皿,燭台,ポットなど多種多様な銀食器が製造されている。銀を宝飾品などで利用する場合,純銀では傷つきやすく,酸化し易いため,他の金属(銅など)との合金の形で利用されることが多い。
銀単体の光反射率はすべての金属の中で最高である。この性質を利用し,鏡や反射フィルムなどに用いられる。
銀単体は,常温での電気抵抗率が既知の金属の中で最も低く,展性・延性が金に次いで高い。この性質を利用し,電気伝導率の良い電線としてオーディオケーブルやスピーカーケーブルなどに,継電器(リレー)の接点表面のめっき材として利用されている。
最近は,太陽光発電の進展に伴い太陽電池用途(銀ペースト,配線など)が増えている。他には,金属をろう付けする際の銀ろう(銀はんだ),食品用途の銀箔などもある。
化合物としての用途
フィルムカメラが主流の時代は,写真の感光剤(臭化銀やヨウ化銀など)としての使用量が多かった。
銀イオンはバクテリアなどに対して強い殺菌力を示し,抗菌加工品に銀化合物を添加したものが用いられる。
ページの先頭へ
金( Au )
金は,埋蔵量は少ないが,地殻内に広く分布している。金鉱石は,通常銀鉱物を伴うため金銀鉱として存在する。金のクラーク数 5×10-7 と白金と同じであるが,レアメタルには分類されていない。
これは,レアメタルの定義(経済産業省)「地球上の存在量が稀であるか,技術的・経済的な理由で抽出困難な金属のうち,安定供給の確保が政策的に重要」により,希少性の他に産業での利用価値が考慮される。すなわち,触媒などで珍重される白金とは異なり,貴金属,貨幣としての用途が主の金はレアメタルの対象にはならない。
金の生産
金鉱床
天然では,金含有量 94.3~100 重量%の自然金,銀との合金であるエレクトラム( 16.9 ~ 94.3重量%)として産出される。これらは,一般的に細粒のため,肉眼で確認できない場合が多い。
天然の金の鉱石・鉱物には,上記のもの以外に次のものがある。
元素鉱物 :オーリキュプライド( Cu3Au )
硫化鉱物 :ウイッテンボガード鉱( Ag3AuS2 )
テルル化鉱物 :カラベラス鉱( AuTe2 ),クレンネル鉱,シルバニア鉱( AuAgTe4 ),ペッツ鉱( Ag3AuTe2 )
セレン化鉱物 :フィッシェライト( Ag3AuSe2 )
アンチモン化鉱物 :安金鉱( AuSb2 )
金の精錬
過去のゴールドラッシュと呼ばれた時代は,自然金の採掘が主流で,金鉱山の金の鉱脈や鉱染(鉱物が散点しているが,全体として特定の鉱物が濃集している鉱床)に沿って掘る方法,金を含む鉱石が風化した砂状のもの(砂金)を回収する方法が用いられていた。
現代では,これらの方法は亜流となり,製錬技術の向上と共に,銀と同様に,銅,鉛,亜鉛などの電解製錬工程の副産物から回収するのが主流となっている。
前出の銅精錬で溶剤として用いるケイ砂( SiO2 )の代わりに金銀鉱を用いると,銅精錬過程で金・銀が粗銅に溶け込む。
粗銅の電気精錬過程で,金と銀は銅から分離され,ほぼ完全に回収することができる。
金単体の特性
金単体は,面心立方構造が安定で,熱伝導性に優れ,電気抵抗率の小さい,光沢のある黄色(金色)の金属である。
柔らかく,展性と延性に富み,非常に薄く( 0.1 μm 程度)仕上げることができる。平面状に延ばしたものを「金箔」(きんぱく),糸状( 1g を 3km まで)に延ばしたものを「金糸」(きんし)と呼ぶ。
反応性
金のイオン化傾向は,全金属中で最も小さく,化学的に非常に安定で,熱,水,酸素,通常の酸・塩基に対して安定に存在する。
しかし,王水(濃塩酸:濃硝酸= 3:1 ),ヨウ素を含むヨードチンキ,熱濃セレン酸,シアン化物の水溶液に対しては溶解する。次に,王水との反応過程を紹介する。
王水中では,硝酸の酸化力により,塩化ニトロシル( NOCl ),塩素( Cl2 )と水が生成する。
HNO3 + 3HCl → NOCl + Cl2 + 2H2O
金と塩化ニトロシル,塩素,塩酸が反応して,一酸化窒素を発生しながら錯体を作り金単体は溶解する。
Au + NOCl + Cl2 + HCl → H ( AuCl4 ) + NO↑
用途例
金の純度は K(カラット)で表記する。1K = 100 /24% ≒ 4.17%で表記する。すなわち,純粋な金は 24K ,金 75%の合金は 18K となる。
金属素材としての用途
金とその合金は,その見栄えの良さや化学的特性を利用して,金糸の刺繍,指輪などの装飾品,美術工芸品,宗教用具,貨幣,メダルなどに用いられてきた。
金属加工用途の金は,過度に軟らかいため,銅,銀などとの合金で用いられる。合金に用いる金属種と量で,金合金の色が変化(カラーゴールド)する。
実用される金・銀・亜鉛の合金には,金箔( 23K :金94.43 , 銀 4.90 , 亜鉛 0.66 ),金色のイエローゴールド( 18K :金75.00 , 銀 15.00 , 亜鉛 10.00 ),ピンクゴールド( 18K :金75.00 , 銀 10.00 , 亜鉛 15.00 ),レッドゴールド( 18K :金75.00 , 銀 - , 亜鉛 25.00 ),グリーンゴールド( 18K :金75.00 , 銀 25.00 , 亜鉛 - ),ホワイトゴールド( 14K :金58.33 , 銀 41.67 , 亜鉛 - )がある。他に,紫色のパープルゴールド( 19K :金80.00 , アルミニウム 20.00 )などもある。
工業的には,電気抵抗率が小さいことに加え,延性が高く細線加工が容易なため,集積回路,電子部品の導線などに,銀より化学的に安定(耐腐食性が高い)なため,高級コネクタ表面のめっき材として用いられる。
化合物としての用途
金化合物と酸化スズ(Ⅱ)( SnO )は,ガラスの着色(金赤)に用いられる。最近に,金コロイド(粒径 0.3μm 程度)の色素として応用研究がある。
ダームスタチウム( Ds )
レントゲニウムは,原子番号 111 ,原子量 (281) の人工放射性元素である。物理的,化学的性質は不明である。レントゲニウム 281 が半減期 26秒と最も長い。
ドイツの重イオン研究所で線形加速装置を用いて作られた。元素名は,X線発見後 100年目に発見されたことから,ドイツの物理学者ヴィルヘルム・レントゲンに因んで命名されたといわれている。
ページの先頭へ