第五部:有機化学の基礎 アルコール・カルボン酸
☆ “ホーム” ⇒ “生活の中の科学“ ⇒ “基礎化学(目次)“ ⇒
ここでは,カルボン酸の基本的な特性に関連し, 【酸としての性質】, 【有機酸の酸性度】, 【置換基効果とは】, 【参考:有機酸】 に項目を分けて紹介する。
酸としての性質
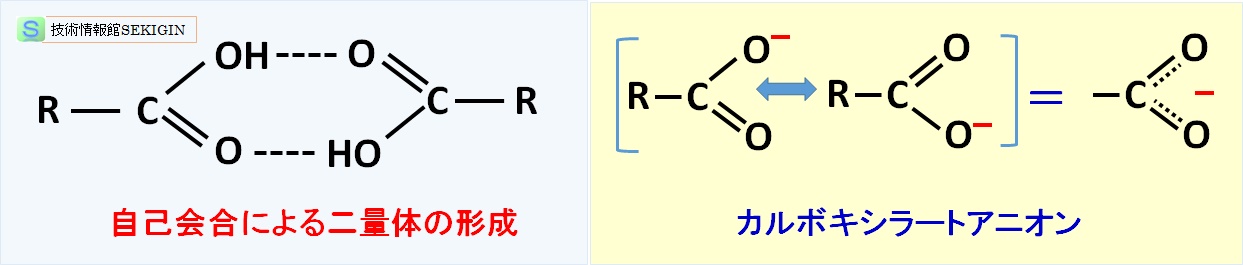
カルボン酸の沸点は,炭素数が同じアルコールやアルデヒドより高い傾向にある。これは,カルボン酸が水素結合により自己会合し,下図に示す二量体を形成するためと考えられる。すなわち,沸騰は,分子間の結合に加え,二量体の水素結合を引き離すエネルギーが必要なため,より高い温度が必要になる。
また,カルボキシ基は,水溶液中でわずかに電離して弱い酸性を示す。
R–COOH + H2O ⇆ R–COO- + H3O+
R–COO- は,カルボキシラートアニオン( carboxylate )といい,実際には,図に示すように陰電荷が 2 つの酸素に非局在化することで安定化する。これが,アルコールより容易に解離できる理由である。
カルボン酸より酸性度の低い酸の塩,例えば炭酸塩やフェノール塩と反応し,二酸化炭素やフェノールを生成する反応が起きる。
R–COOH + NaHCO3 → R–COONa + H2O + CO2↑
R–COOH + C6H5ONa → R–COONa + C6H5OH
なお,ちなみに化合物の酸性度の準位は,概略で無機強酸,有機スルホン酸>カルボン酸>炭酸>フェノールである。
複数のカルボキシ基を持つジカルボン酸やトリカルボン酸などの多価酸は,逐次解離するので,複数の電離定数を持つ。
従って,これらの水溶液の, pH 計算や中和滴定では,逐次の解離を考慮する必要がある。
カルボン酸の特徴
ページの先頭へ
有機酸の酸性度
酸性度とは,酸の強さを表す尺度で,一般的には水素イオンの濃度指数 pH が用いられるが,pH は濃度に依存するため,濃度に依存せず,溶媒を加味した電離定数の負の対数 pKa (酸解離定数)を用いて評価するのが一般的である。なお,pKa が小さいほど酸性度が高いと評価される。
既に述べたように,ギ酸( HCOOH )pKa = 3.77 ,酢酸( CH3COOH )pKa = 4.76 ,プロピオン酸( C2H5COOH )pKa = 4.88 と脂肪酸の pKa は,アルキル基が長くなるほど大きく,すなわち酸性度が低下する(置換基効果)。
また,ジカルボン酸のシュウ酸( HOOC–COOH ) pKa1 = 1.27 ,マロン酸( CH2 (COOH)2 ) pHa1 = 2.83 は,同じ炭素数のモノカルボン酸である酢酸やプロピオン酸より酸解離定数が小さく,カルボキシル基の数が多いほど酸性度が高くなる。
ページの先頭へ
置換基効果とは
ハロゲン( X )などの電気陰性度の大きい元素など電気求引性の置換基( –X , =O , ≡N など)を持つことで,負電荷の非局在化でカルボキシラートアニオンが安定化し,酸性度が上昇する。
逆に,カルボキシラートアニオンを不安定化するアルキル基などの電子供与性の基などがあると,酸性度が低下する。
例えば,酢酸( CH3COOH )の pKa = 4.76 に対し,クロロ酢酸( CH2ClCOOH )pKa = 2.86 ,ジクロロ酢酸( CHCl2COOH )pKa = 1.29 ,トリクロロ酢酸( CCl3COOH )pKa = 0.65 ,トリフルオロ酢酸( CF3COOH )pKa = 0.5 とハロゲンの数や種類により酸性度が変化する。
ページの先頭へ
参考:有機酸
有機化合物の酸の総称を有機酸( Organic acid )という。カルボキシル基( -COOH )を持つカルボン酸が有機酸の代名詞のように扱われるが,他にスルホ基( –SO3H ),ヒドロキシ基( –OH ),チオール基( –SH ),エノール(アルケンの二重結合の片方の炭素にヒドロキシ基が置換したアルコール)を特性基として持つ酸がある。
この中で,スルホ基を持つ有機酸は,強酸に分類されるものが多く,その他の有機酸はの多くは弱酸性化合物である。なお,生化学の分野では有機酸の定義が若干異なり,酸性を示すからといって有機酸に分類しない場合もある。
無機酸(鉱酸)は水に溶解し容易に電離するが,有機溶媒に対してほとんど溶解しない。一方,有機酸は,一部の有機酸を除き,水への溶解性が小さく,有機溶媒への溶解性が高い。このため,有機合成化学ではよく使われる。
スルホ基を持つ強酸(有機スルホン酸)の例
メタンスルホン酸(methanesulfonic acid:CH3SO3H)pKa =-1.9
もっとも単純な有機スルホン酸の一種で,メシル酸( Mesylic acid :MSA)ともいう。強酸性のため脱水縮合反応の酸触媒や医薬品塩の酸成分として利用される。
ベンゼンスルホン酸(benzenesulfonic acid:C6H5SO3H)pKa=-2.8
ベシル酸( Besyl acid )ともいわれる。
パラ(p) -トルエンスルホン酸(p-toluenesulfonic acid:CH3C6H4SO3H)pKa =-2.8
トシル酸(Tosic acid:PTSA,TSA)ともいわれ,有機合成において酸触媒として用いられる。
ページの先頭へ