第五部:有機化学の基礎 有機化合物の分析
☆ “ホーム” ⇒ “生活の中の科学“ ⇒ “基礎化学(目次)“ ⇒
ここでは,核磁気共鳴( NMR )を用いた分析法に関連し, 【化学シフトとは】, 【基準物質との周波数差】, 【スピン-スピン結合定数】, 【 NMR の測定と用途】 に項目を分けて紹介する。
核磁気共鳴:化学シフトとは
化学シフト( chemical shift )
原子核周囲の電子による遮蔽で,原子核に作用する有効磁場に違いが生じ,共鳴周波数の微小な変化をいい,測定対象の原子周辺の化学的状態(構造)に関する情報を得ることができる。
化学シフトは,基準物質の吸収周波数と試料の吸収周波数を測定し,その周波数の差を分光器で設定した変動磁場の周波数で割った値
δ=(試料の吸収周波数 − 基準物質の吸収周波数)/(分光器の周波数)
で表す。
NMR 装置の静磁場の磁束密度 5 T(テスラ)とすると,1H の共鳴周波数 212.9 MHz となる。この周波数が分光器の周波数とした時,一般的な有機化合物の測定では,基準物質との周波数差が数ヘルツから数百ヘルツの間になる。
従って,化学シフトδの値は,10-6 オーダーとなる。このため,測定結果の表記には,百万分の一を意味する ppm で表すのが通例である。
一例として,テトラメチルシラン( TMS : Si (CH3)4 )を基準物質とした時の酢酸メチル( CH3C(O)OCH3 )の 1H NMR スペクトルを下図に紹介する。
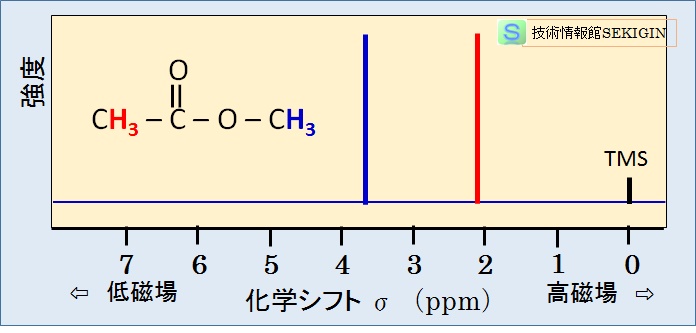
化学シフト測定例(酢酸メチルの 1H NMR スペクトル)
TMS :基準物質
【参考】
化学シフト(NMR)( chemical shift )
核磁気共鳴において,原子核周りの電子状態や原子間の結合状態の違いにより,共鳴周波数がわずかに変化する現象である。核磁気共鳴法の測定結果を用いて,原子核周囲の電子の遮蔽効果による共鳴周波数の微小な変化を解析し,原子周辺の状態など化学構造に関する情報を得ることができる。
ページのトップへ
基準物質との周波数差
基準物質とは
化合物に含まれる測定対象の原子を囲む軌道電子の状態(結合状態)に差のない物が基準物質として選ばれる。例えば,1H ,13C を測定対象とする場合にはテトラメチルシラン( TMS : Si (CH3)4 )が基準物質として用いられる。
TMS( Tetra Methyl Silane )が基準物質に用いられる理由には,1H ,13C NMR で鋭い一本の吸収線を与え,試料のスペクトルへの影響が少なく,安定で高い揮発性を持ち測定後の除去が容易なことが挙げられる。
1H の通常の測定で,溶媒として水素を含まないジュウテリオクロロホルム( CDCl3 )を用いる場合は,基準物質を内部標準として試料溶液に溶解する。
溶媒として重水( D2O )を用いる試料では TMS が溶解しないので,外部標準とするか別の物質が用いられる。
場合によっては,溶媒自身のピークが基準に用いられることもある。
基準物質との周波数差
装置で設定した外部静磁場( B0 )を分子に作用させた時,原子核の周りを覆う電子雲の影響を受け,核に作用する有効磁場( B )は,装置で設定した磁場とは異なるのが通例である。
具体的には,電子は負の電荷を持つ軽い荷電粒子である。外部静磁場に対し【質量分析】の原理で紹介したように,荷電粒子はローレンツ力を受け,磁場に垂直な面で円運動(サイクロトロン運動)する。このため,軌道電子は,軌道運動の変化ではなく電子運動の“揺らぎ”として影響を受ける。
これにより,外部磁場と反対方向に局部磁場( B' )が生じる。これを,電子による遮蔽( shielding )という。
すなわち,原子核に作用する有効磁場( B )は,装置設定の外部静磁場( B0 )と次の関係になる。
B = B0 – B'
基準物質の有効磁場( B1 )と測定対象の有効磁場( B2 )の違いは,核の周りの電子雲の状態の違いによるといえる。
例えば,電気陰性度の大きい元素などを持つ電子求引性官能基を持つ分子では,母体の水素原子周りの電子密度が減るので遮蔽が弱く局部磁場が小さくなり,有効磁場と外部静磁場との差が小さくなる。
その影響は,官能基に近い水素原子と遠い水素原子では異なり,官能基からの距離に依存する。従って,分子に結合する水素は,結合位置により有効磁場が異なることになる。
電子求引性官能基により局部磁場が小さくなった水素原子の有効磁場( B2 )は,基準物質として用いた TMS ( Si(CH3)4 )の水素原子の有効磁場( B1 )と比較すると B1 < B2 となる。
すなわち,それぞれの水素の共鳴周波数(ν=γB /2π )に影響を与え,ν1 < ν2 となる。
分光器の周波数ν0 とすると,化学シフトδの定義により,
δ= (ν2 −ν1 ) /ν0 = ( B2 − B1 ) /B0
の関係が得られる。
化学シフトδの+が大きいことは,基準物質より水素核周りの電子密度が低く共鳴周波数が高いことを意味する。
これは,基準物質の共鳴周波数と同じ周波数で共鳴するためには,低い外部静磁場が必要であることをも意味する。
このため,横軸に化学シフトδ,縦軸にエネルギー吸収の強さをプロットした場合に,上図の例に示すように化学シフトδのプラス方向を低磁場側,マイナス方向を高磁場側と表現する。
なお,ほとんどの有機化合物において,1H NMR の吸収は,TMS の水素の吸収から 0 ~ 10 ppm 低磁場側で起こり,ほとんどの 13C NMR の吸収は,TMS の炭素の吸収から 1 ~ 220 ppm 低磁場側で起こる。
ページの先頭へ
スピン-スピン結合定数
前述の測定例として取り上げた下図に再掲する酢酸メチルは 6 個の水素を有するが,NMR スペクトル図では赤と青の 2本の吸収しか観察されない。赤の吸収線は図中の赤字の水素 3個に依存し,青の吸収線は青字の水素 3個に依存する。

化学シフト測定例(酢酸メチルの 1H NMR スペクトル)
TMS :基準物質
スピン―スピン分裂( spin – spin splitting )
化合物によっては,水素の吸収が多重線( multiplet )としてあらわれる場合がある。例えば,ブロモエタン( CH3CH2Br )の 1H NMR の吸収は,赤字の水素が高磁場側に三重線として,青字の水素は低磁場側に四重線としてあらわれる。
なお,多重線が観察される場合に,多重線の間隔はアルカンで 8Hz未満が多い。この値は,静磁場 5Tの NMRにおける化学シフトδ1ppm (周波数差約 213Hz )に比較して十分に小さいく,通常の NMRスペクトル図表記では多重線が重なり一本のように見える。
この多重線は,スピン―スピン分裂と呼ばれ,多重線の間隔はスピン結合定数 J と呼ばれる。
多重線の発生は,化学シフトで紹介した電子雲による遮蔽の他に,何らかの力が働いていることを示す。
スピン―スピン分裂の原理は, 【核磁気共鳴とは】で紹介した外部磁場による核スピンの分裂に起因する。
分子中のある核種( 1H )に化学的に等価でない核種( 1H )が近接して存在するとき,ある核種( 1H )によって作られる微小磁場が,隣接する核種( 1H )が感じる磁場に影響を与える。
見方を変えると,同時に,隣接する核種( 1H )の作る微小磁場がある核種( 1H )の感じる磁場に影響を与える。この関係をカップリング( Coupling )という。
1H NMR のスピン―スピン分裂(原則)
● 化学的に等価な核種( 1H )はスピン-スピン分裂を示さない。
● 2 個以上の炭素原子を隔てた核種( 1H )は通常カップリングしない。
● ある核種( 1H )と相互作用する隣接する核種( 1H )が n 個の時,ある核種( 1H )の吸収線の数は n + 1 個になる。これを一般的には, n + 1 則という。また,吸収線の強度比は ( x + 1 )n の 展開式の係数比になる。
● 互いに作用した核種のスピン結合定数 J は同じ値を持つ。
例:ブロモエタン( CH3CH2Br )
ある核種( CH3 の 1H )と近接する化学的に等価でない核種( CH2 の 1H )は 2 個なので,ある核種( CH3 の 1H )の吸収線の数は 3 (= 2 + 1) 個(三重線)になる。
吸収線の強度比は,( X + 1 )2 の展開式 X2 + 2X + 1 の係数比 1:2:1 になる。
同様にして,ある核種( CH2 の 1H )と近接する化学的に等価でない核種( CH3 の 1H )は 3 個なので,ある核種( CH2 の 1H )の吸収線の数は 4 (= 3 + 1) 個(四重線)になる。
吸収線の強度比は,( X + 1 )3 の展開式 X3 + 3X2 + 3X + 1 の係数比 1:3:3:1 になる。
このように,スピン―スピン分裂を計測することにより,分子構造に関する情報が得られる。
ページの先頭へ
NMR の測定と用途
NMR は高感度の磁場測定であるため,僅かな要因でスペクトルが歪む。例えば,共鳴周波数が核の感じる磁場(有効磁場)に比例するので,試料周辺の磁場強度の均一度の低下で,吸収線の線幅の広がり,歪みが生じて分解能が低下する。磁場強度の均一度は,装置的な要因(静磁場歪み)の他に試料の不均一な濃度など試料準備にも影響される。
測定時の注意点
● 試料は溶媒に均一に溶解させ,濃度を均一にする。特に高分子材料の試料作製では,低濃度でも粘性が高いので留意が必要である。
● 試料中の不溶物が移動することで,分解能の変動や不安定の原因となるので,ろ過などにより不溶物を可能な限り除去する。
● 試料濃度が高いと粘性が上がり,緩和時間の短縮,分解能の低下に至るので,必要以上に高い濃度としない。
● 試料の量の変化や,装置への装着位置の変化で分解能が影響を受ける。一連の試験では,液量を一定( 誤差 0.2 cm 以内)にし,コイル中心と試料中心が一致するように装着する。
● 試料中に常磁性物質(金属イオン,有機ラジカル,溶存酸素など)が存在すると,電子スピンと核スピンの強い相互作用が生じ分解能が低下する。溶存酸素は窒素置換などで除去する。特に低分子量の測定で注意が必要である。
主な用途
一般的な有機化合物やタンパク質などの複雑な有機化合物の全体構造解析,微細構造解析,定量分析などに用いられる。また,医療診断に用いる MRI も核磁気共鳴を利用したものである。
有機構造解析
1H–NMR ,13C–NMR の1次元測定,2次元測定を用い,有機化合物の分子構造解析,高分子材料の末端基や劣化変性部位の解析,分子間相互作用の解析などが行われる。タンパク質の立体構造解析では,15N 核を含む多次元 NMR 測定を用い,水素原子間距離などの情報から高次構造を求める。
定量測定
吸収スペクトルの強度(積分強度)で試料中の各成分の化学組成や絶対濃度を算出することができる。
緩和時間測定
分子運動性,樹脂の架橋密度や分子量などで変化する緩和時間を解析することで,試料間での架橋密度や分子量の比較ができる。また,緩和時間の温度依存性から分子や原子の運動性を評価できる。
医学的用法
核磁気共鳴現象を利用して生体内の内部の情報を画像にする核磁気共鳴画像法( magnetic resonance imaging : MRI )が用いられている。
医療検査で利用される核磁気共鳴画像法( MRI )は,核磁気共鳴においてパルス照射後の緩和時間(定常状態に戻るまで)が,生体を構成している水分子の運動状態(体内の臓器により異なる)を反映することを利用したものである。
核磁気共鳴画像法では,各組織の緩和時間の違いを,距離に比例した強度を持つ磁場(勾配磁場)をかけ,得られた信号の二次元,又は三次元のフーリエ変換により,個々の位置の信号に分解し画像を描き出す。
ページの先頭へ