第二部:物質の状態と変化 気体の量と体積
☆ “ホーム” ⇒ “生活の中の科学“ ⇒ “基礎化学(目次)“ ⇒
ここでは,混合気体の状態方程式(分圧の法則,分体積の法則)の実例として,【空気について】, 【空気中の酸素と窒素の関係】 に項目を分けて紹介する。
空気について
混合気体の状態方程式を最も身近な混合気体(空気)を例に適用例を紹介する。なお,一般の空気は,気象情報の中で,相対湿度で表現されるように,地域,時間により含まれる水分量が大きく異なる。このため,空気の組成を問題とする場合は,水分量を除いた乾燥空気について表現される。
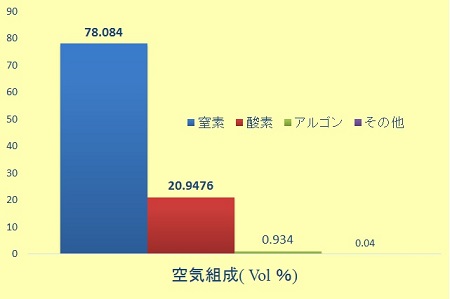
空気の組成( Vol %)
乾燥空気の組成
次には,国際標準大気( 1975 )として公表されている海面付近(1気圧)の大気成分の値を示す。示された値は,水分,微粒子を除いた清浄な乾燥空気の組成(容量%)である。
水を除く主要成分(%)は,窒素( N2: 78.084 ),酸素( O2: 20.9476 ),アルゴン( Ar : 0.934 )である。
少量成分(%)には,二酸化炭素( CO2 : 0.0390 ),ネオン( Ne : 0.001818 )が挙げられる。
主な微量成分(%)として,ヘリウム( He : 0.000524 ),メタン( CH4 : 0.000181 ),クリプトン( Kr : 0.000114 ),二酸化硫黄( SO2 : 0.0001> ),水素( H2 : 0.00005 ),一酸化二窒素( N2O : 0.000032 ),キセノン( Xe : 0.0000087 ),オゾン( O3 : 0.000007> ),二酸化窒素( NO2 : 0.000002> ),ヨウ素( I2 : 0.000001> )が含まれる。
なお,太字の二酸化炭素,メタン,硫黄酸化物,窒素酸化物,オゾンは,人の産業活動で排出されるため,地域,時間等で濃度が変化する成分である。
実際の大気は,主要成分として水を含む。その量は,次項の【空気中の水分(湿度)】で紹介するように,25℃の相対湿度 60%で約 1.88 容量%となり,アルゴンより多く,酸素に次ぐ量の水が含まれる。
ページのトップへ
空気中の窒素と酸素の関係
乾燥空気に占める窒素と酸素の合計は,99.032 %となる。すなわち,乾燥空気の性質は,窒素と酸素の混合気体と考えて差し支えない。
ここで,乾燥空気における窒素と酸素の体積比,物質量(=分子の数),分圧の関係を求める。なお,大気から浮遊微粒子を除いた乾燥空気は,概ね理想気体として扱えるので,気体の状態方程式を適用する。
乾燥空気の組成(容量%)から窒素と酸素の体積比は,
VN2 / VO2 ≒ 78 / 21
となる。
ある温度でのモル体積( Vm )は分子種によらず一定(例えば,0℃で約 22.414 L / mol )となるので,
Vm = VN2 / nN2 = VO2 / nO2 =一定となる。
∴ nN2 / nO2 = VN2 / VO2 ≒ 78 / 21
となり,物質量の比は体積比と同じになる。
混合気体の状態方程式(分圧の法則,分体積の法則)より,
PN2 V = P VN2 , PO2 V= P VO2 とできる。
∴ PN2 / PO2 = VN2 / VO2 ≒ 78 / 21
となり,分圧の比が体積比と同じになる。
このように,混合気体の体積比,物質量の比,分子量の比,分圧の比は同じであることが分かる。
【参考】
国際標準大気( International Standard Atmosphere, ISA )
地球大気の圧力,温度,密度,および粘性が高度によってどのように変化するかを表したモデル。ISO (国際標準化機構)によって 1975年に ISO 2533 として策定されている。
このほかに,標準大気として,独自の拡張や一部の改変を施したものが他の標準化団体によって策定されている。
標準によれば,海面上の気圧 101.3 kPa ,気温 15 ℃のとき,気温減率(高度による気温低下率)は 6.5 K / km なども規定されている。
ページの先頭へ