腐食概論:腐食の基礎
☆ “ホーム” ⇒ “腐食・防食とは“ ⇒ “腐食概論(腐食の基礎)” ⇒
ここでは,腐食現象に関連し, 【均一腐食:汚染表面の濡れ】, 【主な用語】 を紹介する。
腐食現象の分類
均一腐食:汚染表面の濡れ
金属表面が海塩粒子(sea-salt particle)などの塩類で汚染されている場合は,清浄表面の場合より低い相対湿度で厚い水膜に覆われる。この主な原因は,塩の潮解(deliquescence)による。
海水中の塩の組成比は,海域が異なってもほぼ一定で,塩化ナトリウム( NaCl )77.9%,塩化マグネシウム( MgCl2 )9.6%,硫酸マグネシウム( MgSO4 )6.1%,硫酸カルシウム( CaSO4 )4%,塩化カリウム( KCl )2.1%,残分がその他成分となっている。
常温(25℃程度)で各塩の潮解し始める相対湿度(relative humidity)は,MgCl2 で約 33RH%,NaCl が約 75RH%,KCl では約 84RH%,MgSO4 で約 93RH%である。硫酸カルシウム(いわゆる石膏)は,溶解度が約 2g/lと低く,いわゆる潮解現象を考慮する必要はない。
金属腐食の観点からは,前項で紹介した清浄表面で濡れに至らない相対湿度 80RH%以下で潮解する塩の付着が問題となる。
押川らは,模擬海塩( NaCl+MgCl2 )の付着した表面における水膜厚みと相対湿度の関係を推定している。
この結果は,下図に示すように,表面い付着する水膜の厚みは,MgCl2 の潮解が開始する相対湿度 33%で急増する。
その後,NaClの潮解が始まる相対湿度 75%までは,MgCl2 水溶液の蒸気圧バランスに応じ緩やかに増加する。
相対湿度が 75%に至ると,固体として残っていたNaClの潮解が開始するため,再度急激な水膜厚みの増加に至る。
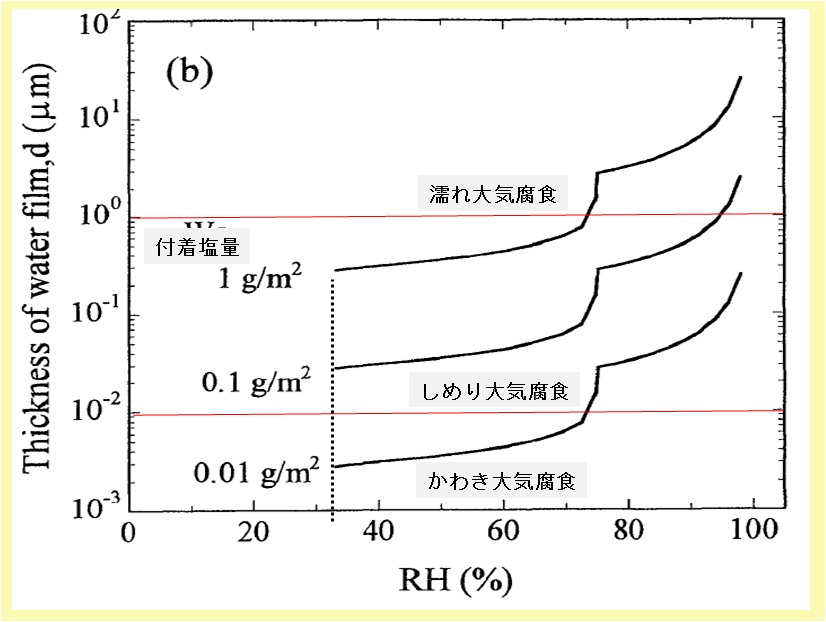
海塩付着鋼表面の相対湿度と水膜厚み
出典:押川渡,篠原正,元田慎一:“強電解質が吸水してできる水膜組成と水膜厚さの推定”,材料と環境,Vol.52, No.6 pp. 293-298(2003)
ページのトップへ
主な用語の概説
海塩粒子(sea-salt particle)
海岸の波打ち際及び/又は海上で波頭が砕けたときに発生する海水ミストが,風で運ばれて飛来した粒子。海塩粒子の大きさは,約 0.01μm~20μm である。【JIS Z 2381「大気暴露試験方法通則」】
潮解(deliquescence)
対象とする物質(固体)の飽和水溶液の水蒸気圧と問題とする環境の水蒸気の分圧(湿度)を比較し,環境の水蒸気の分圧が大きい場合に,物質が環境中の水分子を吸収し,物質を含む水溶液を形成する現象をいう。
固体が残存している場合は,飽和水溶液を形成する。固体がすべて水溶液になった後は,水溶液の水蒸気圧が環境の水蒸気分圧に一致する濃度まで希釈される。この現象を起こす物質には,塩化マグネシウム(MgCl2), 水酸化ナトリウム(NaOH),塩化カルシウム(CaCl2) ,クエン酸(C6H8O7)などがある。
相対湿度(relative humidity)
相対湿度(RH)とは,ある温度(T)で計測された水蒸気圧(E)と,その温度での飽和水蒸気圧( Es (T))(saturated water vapor pressure) に対するの百分率と定義されている。
RH(%)=100×E/Es (T)
絶対湿度(absolute humidity)
水蒸気量を直接示すために用いられる。一般的には,大気の一定体積(1m3)当たりの水蒸気の量(g)で表わす容量絶対湿度 VH(volumetric humidity ; g/m3)で表される。
すなわち,容積 Va(m3)に含まれる水蒸気の質量を Mw(g)とすると,容量絶対湿度 VH=Mw/Va で定義される。
相対湿度 RH との関係は,T:温度(℃),E:水蒸気圧,Es(T):飽和水蒸気圧,とした場合に次式で与えられる。
VH= (RH/100)・Es(T)・216.7/(T+273.15)
飽和水蒸気圧(saturated water vapor pressure , saturated steam pressure)
気象学において,水蒸気が気液平衡にある場合の蒸気圧をいい,一般的には平衡蒸気圧(へいこうじょうきあつ)という。
なお,地表付近(一気圧),温度 T(℃)の飽和水蒸気圧は,Es(T) ≒ 6.1078・exp{ 17.27・T/(T+237.3)} で近似できる。
ページのトップへ