第六部:生化学の基礎 脂質
☆ “ホーム” ⇒ “生活の中の科学“ ⇒ “基礎化学(目次)“ ⇒
ここでは,物質代謝で重要な役割を持つ ATP の生成とクエン酸回路の関係について, 【 ATP とは】, 【 ATP の合成反応】, 【 ATP 生成量】 に項目を分けて紹介する。
ATP とは
ATP (アデノシン 5'-三リン酸)
ヌクレオチドの一種で補酵素に分類される化合物で,3分子のリン酸が付き,2個の高エネルギーリン酸結合をもつ化合物である。
りん酸 1分子の離脱によりエネルギーを放出し,放出した分子がりん酸と結合することでりん酸エネルギーを貯蔵することができる化合物である。また,物質の代謝・合成において重要な役目も果たしている。
すべての真核生物(動植物など細胞の中に細胞核を有する生物)が利用し,エネルギーの放出と蓄積に関わるので,「生体のエネルギー通貨」とも言われている。
ATP の表記は,ヌクレオチドの一種で,五炭糖のリボースであるアデノシン三リン酸( Adenosine TriPhosphate )の赤字のアルファベットを用いた短縮形である。なお,IUPAC 名は,アデノシン 5'-三リン酸である。
ATP は,リボースの 5'-ヒドロキシ基にリン酸エステル結合により 3分子のリン酸が連続して結合した構造のものであるが,1分子のリン酸基が結合したものを AMP( Adenosine MonoPhosphate ,アデノシン一リン酸,アデニル酸),2分子のリン酸基が付いたものを ADP ( Adenosine DiPhosphate ,アデノシン二リン酸)という。
エネルギーの放出
下図に例示するように,ATP や ADP のように,連続したリン酸基同士の結合(リン酸無水結合)は,エネルギー的に不安定なため,リン酸基の加水分解による切断反応,他の分子にリン酸基を転移する反応でエネルギーを放出する。
例えば,ATP + H2O → ADP + Pi(リン酸)で 30.5 kJ /mol ,ATP + H2O → AMP + PPi(ピロリン酸)で 45.6 kJ /molの標準自由エネルギー変化がある。
さらに,細胞内の ATP 濃度は ADP の10倍程高いなど,ATP の加水分解などの反応が自発的に起きる状況にある。
このように,ATP のリン酸基同士の結合切断によるエネルギー変化が,他の生化学反応の推進に寄与するため,この結合を「高エネルギーリン酸結合」とも呼ばれている。
ATP は,エネルギーを要する生体反応に必ずといえるほど使用されている。例えば,解糖系の グルコースのリン酸化など,糖新生などの生合性反応,筋肉のアクチン・ミオシンの収縮,濃度勾配に逆らって物質移動する能動輸送,RNA 合成の前駆体などである。
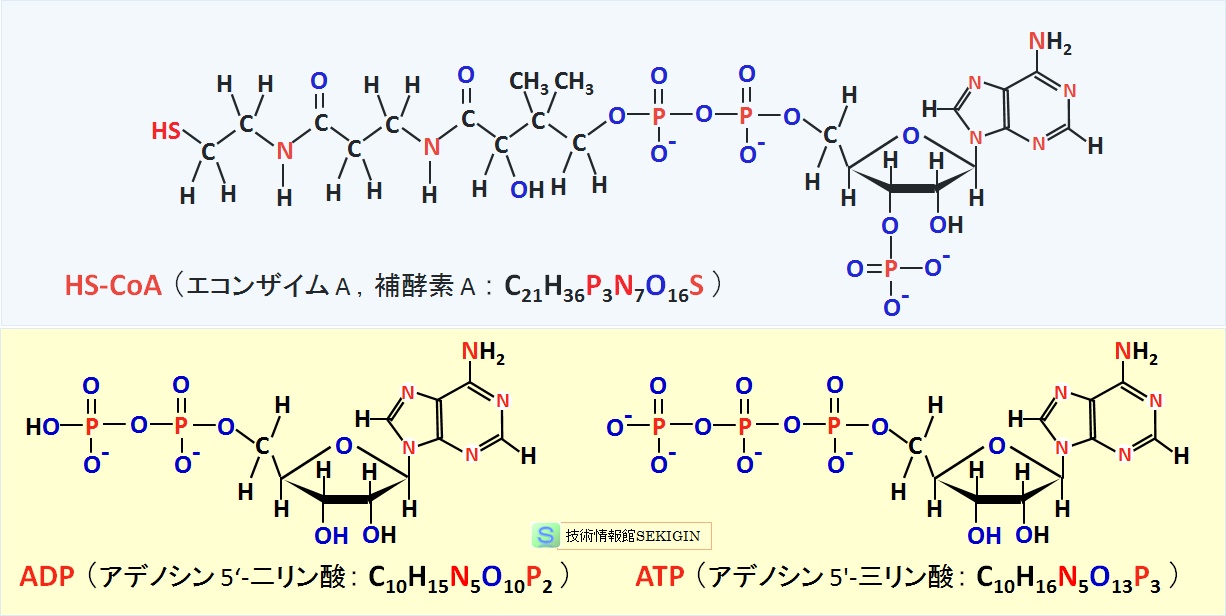
CoA (補酵素A ,コエンザイムA ),ADP,ATP
ページのトップへ
ATP の合成反応
ATP は,解糖系やクエン酸回路などでも ATP は生じるが,主に酸化的リン酸化(ミトコンドリア内の電子伝達系に共役して起こる反応で,水素イオンの濃度勾配を利用した ADPのリン酸化),光合成・明反応における ATP 合成酵素による光リン酸化によって生じる。
光リン酸化( photophosphorylation )
ADP + Pi + H+ → ATP + H2O
また, GTP(グアノシン三リン酸)は,自由エネルギー変化をほとんど伴わずに ATP と相互変換する。
GTP + ADP ⇔ GDP + ATP
酸化的リン酸化( oxidative phosphorylation )
細胞呼吸(好気呼吸)には,大きく分けて,解糖系,クエン酸回路,酸化的リン酸化の 3 つの代謝が関わる。解糖系を要約すると,細胞質基質で行われる酸素を使わない糖の酸化過程で,クエン酸回路は,ミトコンドリアのマトリックスでピルビン酸などから変換されたアセチル CoA を二酸化炭素に分解する酸化過程である。
酸化的リン酸化とは,電子伝達系とも呼ばれ,水素受容体( NADH2+ ,FADH2 など還元型の補酵素)を酸化し,酸素に電子を伝えて水を生成する過程において,光リン酸化と同様に,ATP を生成する反応系である。
具体的には,ミトコンドリアのマトリックス側(内膜の内側)で発生したプロトン( H+ )を膜間スペース(外膜と内膜の間)へ汲み出すことで,ミトコンドリア内膜を隔てて,隙間スペースが高濃度となる H+ の濃度勾配が生じる。このため,マトリックスと膜間スペースの間に電位差が生じる。
この電位差に逆らい膜間スペースからマトリックスへ 3 個のプロトンが流入するときに,ATP 合成酵素により ADP とリン酸から 1 分子の ATP が合成される。
ADP + Pi + H+ → ATP + H2O
なお,“プロトンの汲み出し”に関し,水素受容体( NADH2+ ,FADH2 など)の酸化により,グルコース 1 分子あたり 100 個以上のプロトンがミトコンドリア内膜の外に放出されるといわれている。
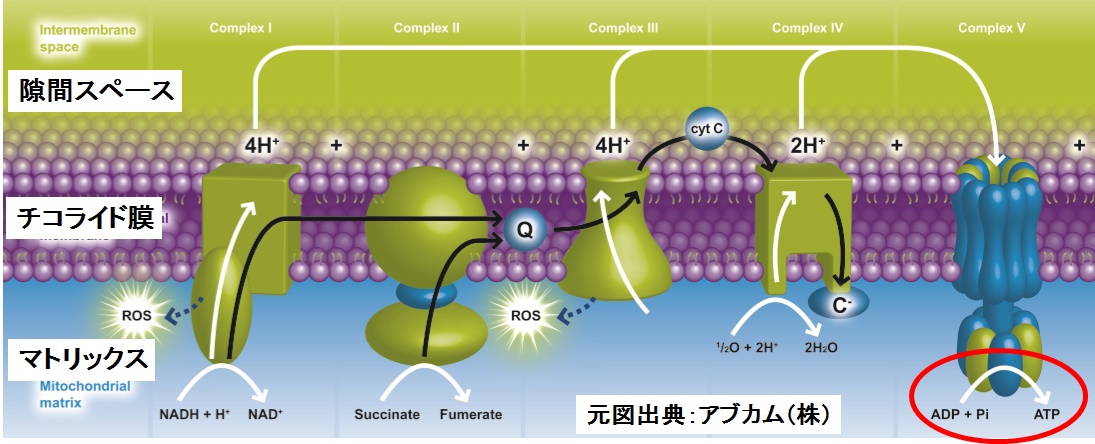
酸化的リン酸化
元図出典:アブカム(株)酸化的リン酸化反応によるエネルギー産生
ページの先頭へ
ATP の生成量
細胞呼吸によるグルコース1分子( C6H12O6 )からの ATP 生成量は,一般的な教科書では 38当量となっている。
C6H12O6 + 6O2 + 38ADP + 38Pi → 6CO2 + 6H2O + 38ATP
この内訳は,
解糖系( 2当量)
C6H12O6 + 2NAD+ + 2ADP + 2Pi → 2C3H4O3 (ピルビン酸) + 2NADH2+ + 2ATP
クエン酸回路( 2当量)
2C3H4O3 + 2NAD+ + 2HS-CoA → 2CH3CO-S-CoA (アセチル CoA ) + 2CO2 + 2NADH2+
2CH3CO-S-CoA + 6NAD+ + 2FAD + 2GDP + 2Pi + 6H2O
→ 4CO2 + 6NADH2+ + 2FADH2 + 2GTP + 2HS-CoA , 2GTP + 2ADP ⇔ 2GDP + 2ATP
酸化的リン酸化( 34当量)
ミトコンドリアの内壁を貫くサブユニットのマトリックス側に存在する ATP 合成酵素によって,膜間スペースからマトリックス側に逆流したプロトン( H+ )により,ADP がリン酸化して ATP ができる。
ADP + Pi + H+ → ATP + H2O
プロトンの逆流は,1当量の NADH2+ から ATP 約 3当量,1当量の FADH2 から ATP 約 2当量の生成が可能といわれている。
すなわち,上述の細胞呼吸(解糖系,クエン酸回路)では,グルコール一分子あたりで,生成する NADH2+ は 10当量,FADH2 が 2当量となるので,最大で 10×3+2×2=34当量の ATP が生成できると計算される。
【参考】
NAD (ニコチンアミドアデニンジヌクレオチド: nicotinamide adenine dinucleotide )
全ての真核生物で用いられる電子伝達体で,脱水素酵素の補酵素として,酸化型( NAD+ )と還元型( NADH )の状態を取り得る。
なお,一般的には( NADH + H+ )の状態を( NADH2+ )と表記する例がおおい。
NADH2+ + 酸化物質 ⇔ NAD+ + 還元物質( 2e- + 2H+ )
FAD(フラビンアデニンジヌクレオチド: flavin adenine dinucleotide )
代謝反応に必要な酸化還元反応の補酵素で,酸化型( FAD )と還元型( FADH2 )の状態を取り得る。
FADH2 + 酸化物質 ⇔ FAD + 還元物質( 2e- + 2H+ )
ページの先頭へ