腐食概論:金属概論
☆ “ホーム” ⇒ “腐食・防食とは“ ⇒ “金属概論” ⇒
金属の基礎
金属の結晶構造
展延性と結合
物体が外力で変形した場合に,食塩などのイオン結合(electrovalent bond)の物質やガラスなどの共有結合(covalent bond)の物質では,結合が破壊し損傷を受ける。しかし,金属結合(metal bond)では結合電子が自由に動き回れる(自由電子(free electron))ため,原子自体の移動も容易で,周りの電子が動ける範囲において,金属結合は破壊されずにすむ。これが,金属特有の塑性(plasticity)や展延性(ductility)に寄与している。
金属の展延性と結晶構造
金属の原子配列は,ほとんどの場合,図に示す面心立方格子構造 (fcc:face-centered cubic lattice),体心立方格子構造(bcc:body-centered cubic lattice),ちゅう密六方格子(hexagonal close-packed lattice)に分けられる。
なお,ちゅう密六方格子(hexagonal close-packed lattice)は,六方最密充填構造 (hcp:hexagonal close-packing)ともいわれる。
結晶構造(crystal structure)の違いは,原子の移動し易さ,すなわち延性(ductility)や展性(malleability)に影響する。
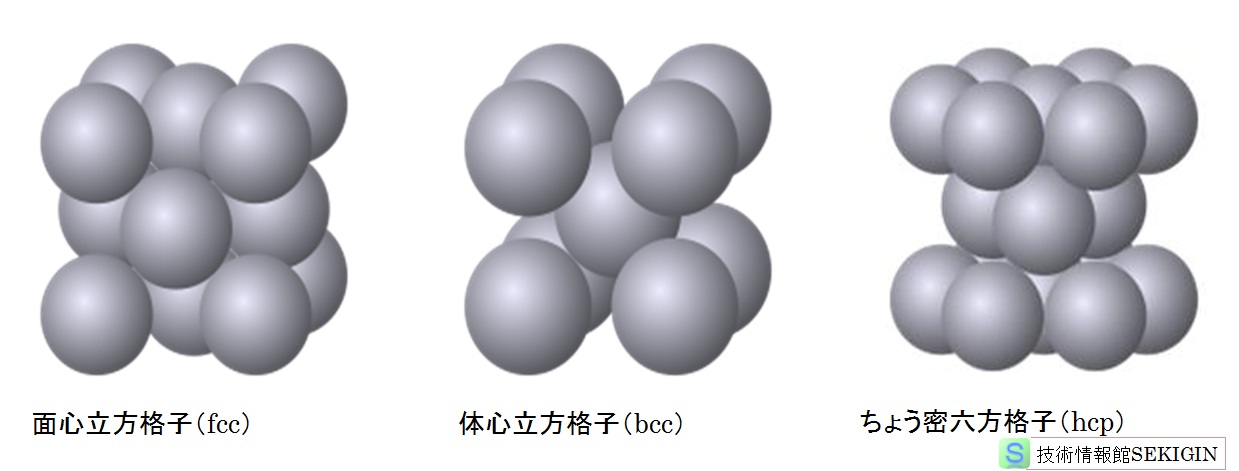
主要な結晶構造
一方,体心立方格子は,面心立方格子を一方向に押しつぶした構造となり,面心立方格子に比較して,原子の面状でのずれ易さで劣り,変形しにくい。
ちゅう密六方格子は,外部の応力に対して,構造上でずれる面が一方向のみとなる。従って,外力に対する“ずれ”の抵抗が大きく,変形し難い。この構造の金属は,硬くて脆い性質を持つ。
【参考資料】
1)大澤直 『金属のおはなし』 日本規格協会,2008年
2) 伊藤尚夫,無機化学シリーズ11「金属元素の化学」培風館,1972年
3) 齋藤勝裕 『金属のふしぎ』 ソフトバンククリエイティブ,2009年
ページのトップへ